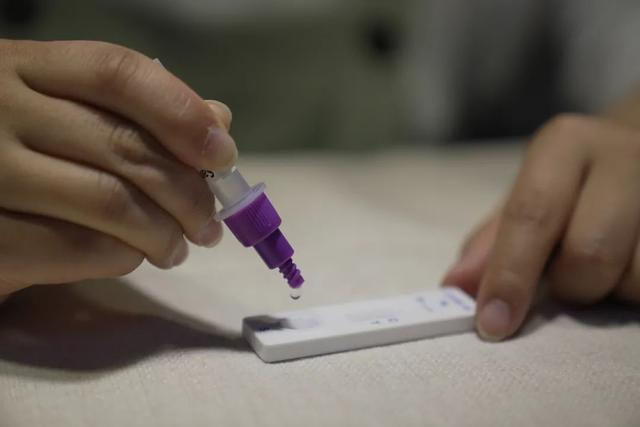
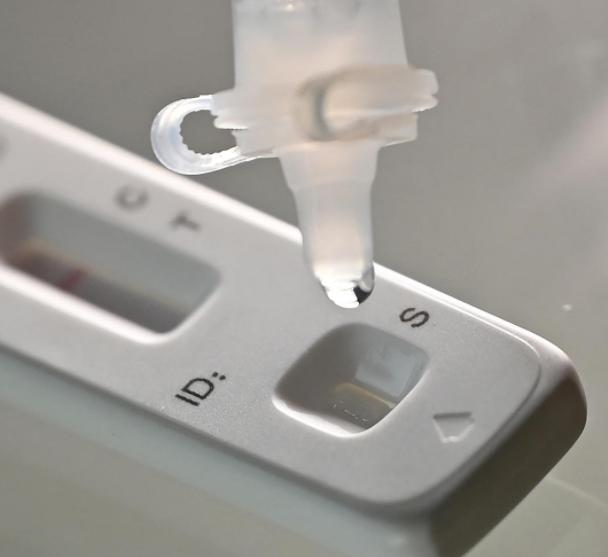
Den 12. marsth 2022, deNMPA (SFDA) utstedt en melding som godkjenner endringen av søknaden om selvtesting av COVID-19-antigenprodukter av Nanjing Vazyme BiotechCo., Ltd, Beijing Jinwofu Bioengineering TechnologyCo., Ltd, Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd ogBeijing Savant Biotechnology Co., Ltd(Huaketai).Fem selvtestende produkter for COVID-19-antigen har blitt lansert.
Den 11. mars 2022 hadde NHC kunngjort at for ytterligere å optimere teststrategien for den nye koronaviruset og imøtekomme behovene for forebygging og kontroll av COVID-19, besluttet det omfattende teamet til den felles forebyggings- og kontrollmekanismen til statsrådet å legge til antigentesting til nukleinsyretesting og laget "applikasjonsprotokollen for ny koronavirusantigendeteksjon (prøve)"
Protokollen spesifiserer den aktuelle populasjonen for antigentesting:
Først de som besøker primærmedisinske institusjoner og har symptomer som luftveier og feber innen 5 dager etter symptomdebut;
For det andre, karanteneobservasjonspersonell, inkludert hjemmekaranteneobservasjon, nærkontakt og sub-nær kontakt, innpasseringskaranteneobservasjon, inneslutningsområde og kontrollområdepersonell;
Den tredje er innbyggerne i samfunnet som har behov for antigen-selvdeteksjon.
Tips: Antigendeteksjon er et viktig supplement til nukleinsyredeteksjon, men resultatene av antigen-selvdeteksjon kan ikke brukes som grunnlag for infeksjonsdiagnose
Innleggstid: 22. mars 2022